Nous rapportons la plus longue persistance documentée à ce jour de composants de vaccins à ARNm, confirmée de manière indépendante par plusieurs laboratoires, échantillons biologiques et points temporels de mesure à l’aide de diverses méthodes d’analyse.
NICOLAS HULSCHER, MPH 2 FÉVRIER 2026
Pendant des années, on a dit au public que les vaccins à base d’ARNm se dégraderaient en quelques jours ou quelques semaines, qu’ils se décomposeraient rapidement, qu’ils seraient biologiquement transitoires et incapables de persister à long terme. Cette hypothèse a façonné les assurances réglementaires, les messages publics et les attentes en matière de sécurité dans le monde entier. Des milliards de personnes à travers le monde ont reçu ces injections sur la base de l’affirmation selon laquelle le matériel génétique disparaîtrait rapidement de l’organisme.
Aujourd’hui, ce récit s’effondre – à la suite d’un effort d’investigation coordonné et multi-pays impliquant la Fondation McCullough, le laboratoire INMODIA (Allemagne), l’hôpital municipal de Dresde-Friedrichstadt (Allemagne), Neo7Bioscience, et des laboratoires indépendants collaborant.
L’article qui en résulte, intitulé « Unprecedented Persistence of Vaccine mRNA, Plasmid DNA, Spike Protein, and Genomic Dysregulation Over 3.5 Years Post-COVID-19 mRNA Vaccination » (Persistance sans précédent de l’ARNm du vaccin, de l’ADN plasmidique, de la protéine spike et de la dysrégulation génomique 3,5 ans après la vaccination par l’ARNm du COVID-19), présente ce qui est, à notre connaissance, le rapport de cas de lésions dues au vaccin COVID-19 le plus complet à ce jour – impliquant plus de 40 visites au service des urgences, plus de 200 rencontres avec des spécialistes dans 18 disciplines médicales, plus de 100 examens de laboratoire, plus de 100 examens d’imagerie et des prélèvements en série de sang et de tissus effectués à de multiples moments sur plus de 3,5 ans.
Les résultats révèlent des preuves moléculaires longitudinales que l’ARNm, les fragments d’ADN plasmidique et la protéine spike dérivés du vaccin peuvent persister dans le sang et les tissus humains plus de 3,5 ans après la vaccination, ce qui a été confirmé de manière indépendante par de nombreux laboratoires utilisant diverses méthodes d’analyse.
L’infection par le SARS-CoV-2 a été effectivement exclue : les anticorps anti-nucléocapside sont restés négatifs à cinq moments différents et dans trois laboratoires indépendants, et la protéine de la nucléocapside était absente des échantillons de tissus malgré la présence d’un dépôt de protéines spike.
Présentation de cas
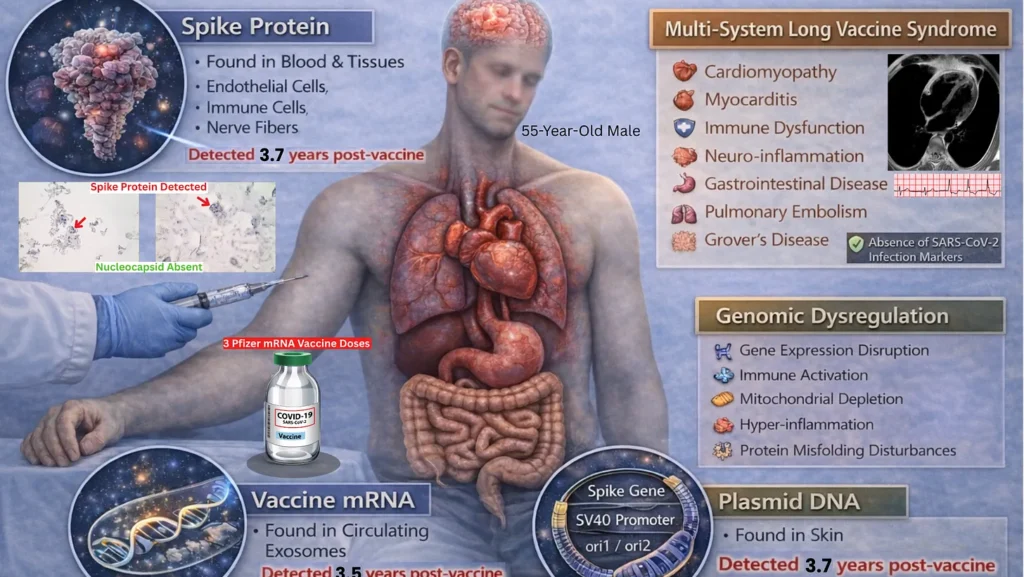
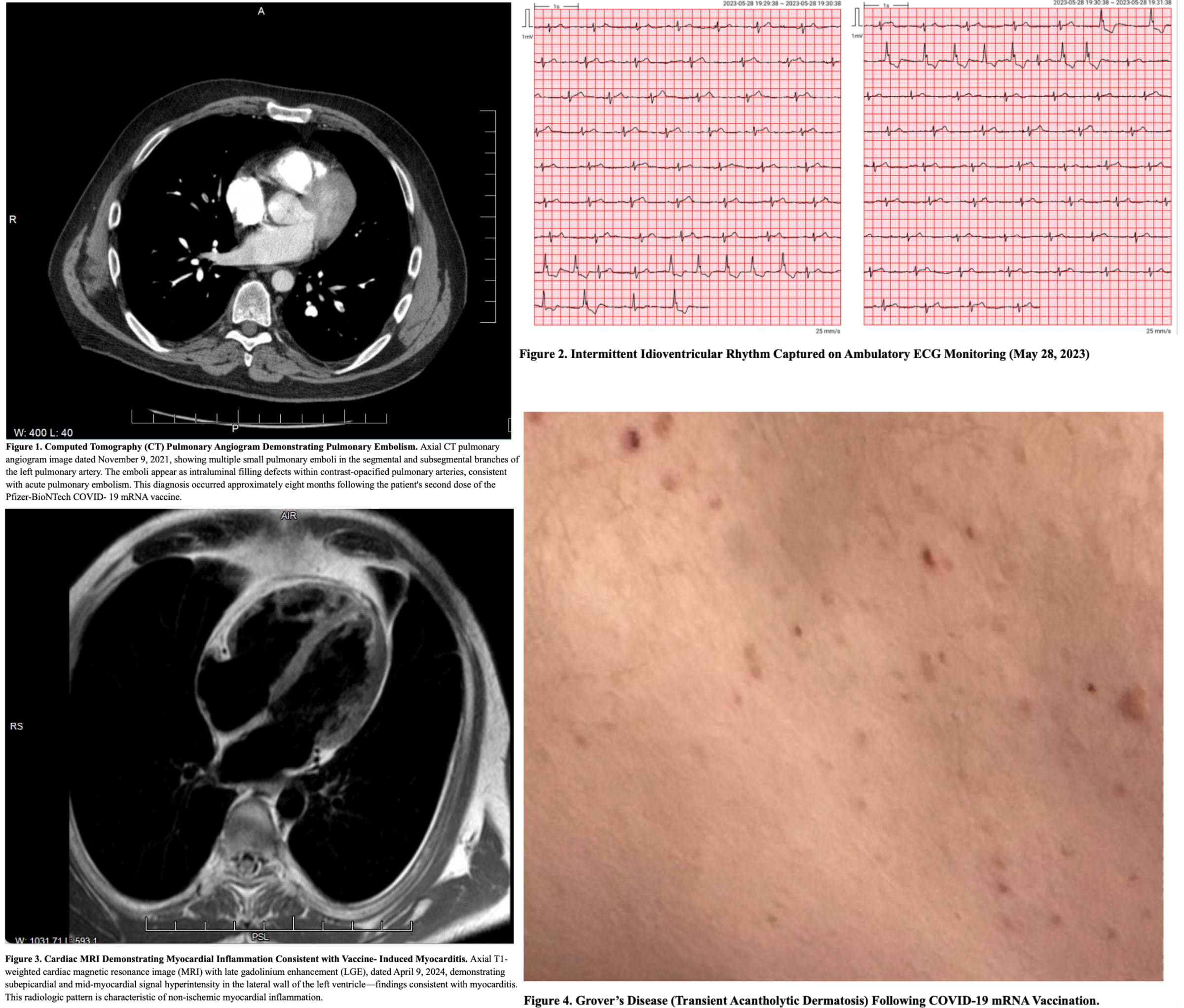
Nous rapportons le cas d’un homme de 55 ans qui a reçu trois doses du vaccin ARNm COVID-19 de Pfizer-BioNTech et qui a développé par la suite un dysfonctionnement progressif de plusieurs organes correspondant au syndrome post-vaccin COVID-19 (SPVC), impliquant les domaines cardio-pulmonaire, neurologique, musculo-squelettique, gastro-intestinal, autonome, otolaryngologique, audiovestibulaire, immunitaire, ophtalmologique, dermatologique et psychiatrique. Les manifestations cliniques comprenaient : des embolies pulmonaires, une myocardite tardive confirmée par IRM, des troubles neurocognitifs, une neuropathie des petites fibres, un dysfonctionnement autonome, des myalgies, une atteinte pancréatique et gastro-intestinale chronique, une aggravation des acouphènes avec perte auditive neurosensorielle, une dysphagie vocale et une dysphonie, des troubles ophtalmiques, une inflammation dermatologique chronique et de l’anxiété/de la dépression. Le cas a été évalué dans le cadre d’une investigation clinique longitudinale et multi-domaine unique, couvrant des analyses moléculaires, immunologiques, génétiques, protéomiques, transcriptomiques et tissulaires, entreprises pour caractériser les mécanismes de la maladie et exclure d’autres étiologies.
Évaluation diagnostique approfondie
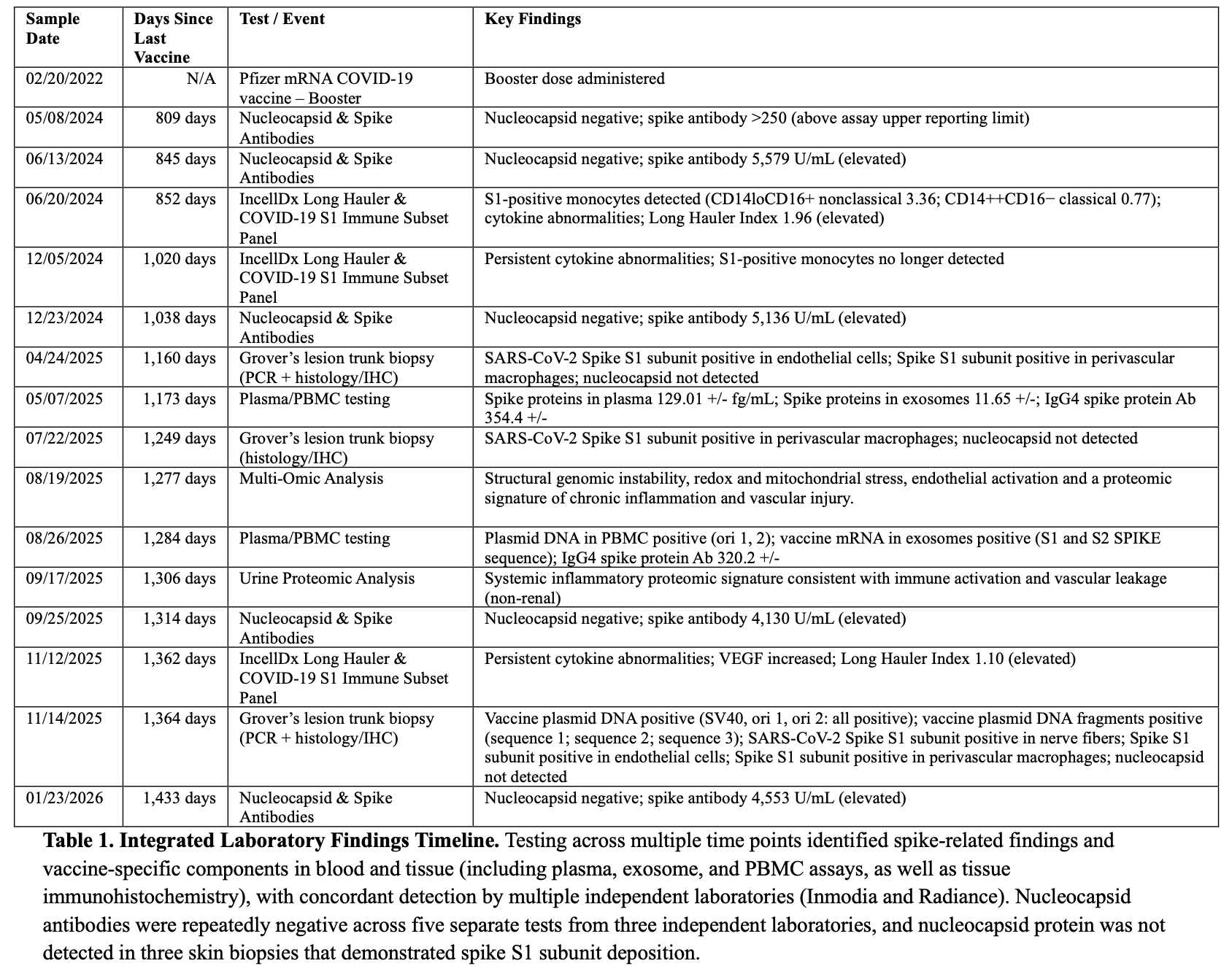
Après plus de 40 visites aux urgences et plus de 200 consultations externes spécialisées, le patient a subi plus de 100 examens de laboratoire non routiniers et plus de 100 examens d’imagerie/fonctionnels. Cette évaluation a systématiquement exclu les mécanismes étiologiques sous-jacents dans les domaines infectieux, auto-immun, rhumatologique, endocrinien, génétique, hématologique, malin, toxique/lié aux médicaments, cardiovasculaire/vasculaire, métabolique et neurologique primaire. Les tests sont restés largement non diagnostiques. Après le diagnostic de myocardite, on a soupçonné l’existence d’une infection asymptomatique non documentée ou non diagnostiquée se manifestant sous la forme d’un COVID long, et on a procédé à une sérologie ; des résultats inattendus ont incité à élargir les tests immunitaires et tissulaires pour rechercher les composants dérivés des pics et des vaccins. Les anticorps de la nucléocapside du SRAS-CoV-2 se sont révélés négatifs à cinq moments distincts, entre 809 et 1 433 jours après la vaccination, ce qui a été confirmé par trois laboratoires indépendants. Le patient reste négatif pour la nucléocapside avec des niveaux d’anticorps de pointe toujours élevés (4 553 U/mL) 1 433 jours après la dernière vaccination.
Collecte d’échantillons et méthodes d’analyse
Des échantillons de sang et de tissu cutané ont été prélevés à plusieurs moments entre 852 et 1 364 jours après la dernière vaccination par l’ARNm COVID-19 de Pfizer-BioNTech. Les compartiments biologiques analysés comprenaient le plasma, les exosomes circulants, les cellules mononucléaires du sang périphérique (PBMC) et les tissus cutanés. Les échantillons ont été évalués par plusieurs laboratoires indépendants en utilisant diverses méthodologies analytiques, notamment ELISA, immunohistochimie automatisée, RT-PCR, PCR standard avec confirmation par séquençage Sanger, séquençage du génome entier, profilage transcriptomique et spectrométrie de masse quantitative.
Protéine spike persistante et ARNm dérivés du vaccin
Quatre-vingt-deux jours après la vaccination, les tests immunitaires sanguins ont permis de détecter la protéine S1 du SRAS-CoV-2 dans les sous-ensembles de monocytes classiques et non classiques, avec les anomalies des cytokines et des marqueurs immunitaires qui y sont associées.
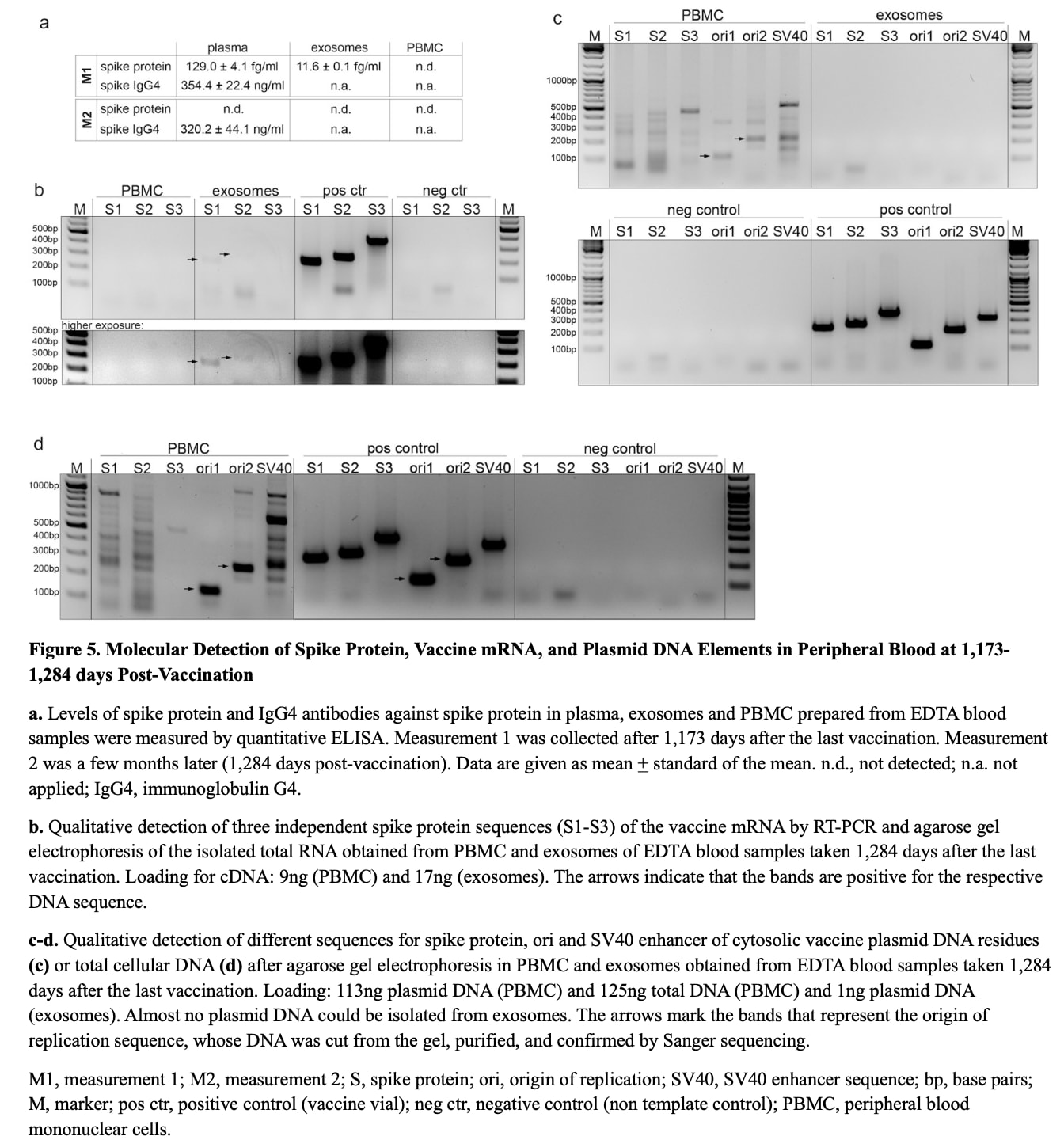
1 173 jours après la vaccination, un test ELISA à haute sensibilité a permis de détecter la protéine Wuhan spike libre dans le plasma (129,0 ± 4,1 fg/mL) et dans les exosomes circulants (11,6 ± 0,1 fg/mL).
À 1 284 jours, la RT-PCR a permis d’identifier l’ARNm du pic dérivé du vaccin dans les exosomes circulants, alors que l’ARN des PBMC est resté négatif après une extraction traitée par DNase et une PCR spécifique de l’amplicon ciblant trois régions de l’ORF du pic (S1-S3).
Le profilage sérologique effectué 1 173 et 1 284 jours après la vaccination a révélé des concentrations toujours élevées d’IgG4 spécifiques du pic (354,4 ± 22,4 ng/mL et 320,2 ± 4,4 ng/mL, respectivement), ce qui correspond à une stimulation antigénique continue et à une réponse décalée par rapport à la tolérance immunitaire.
Protéine spike persistante et ADN plasmidique dans le tissu cutané
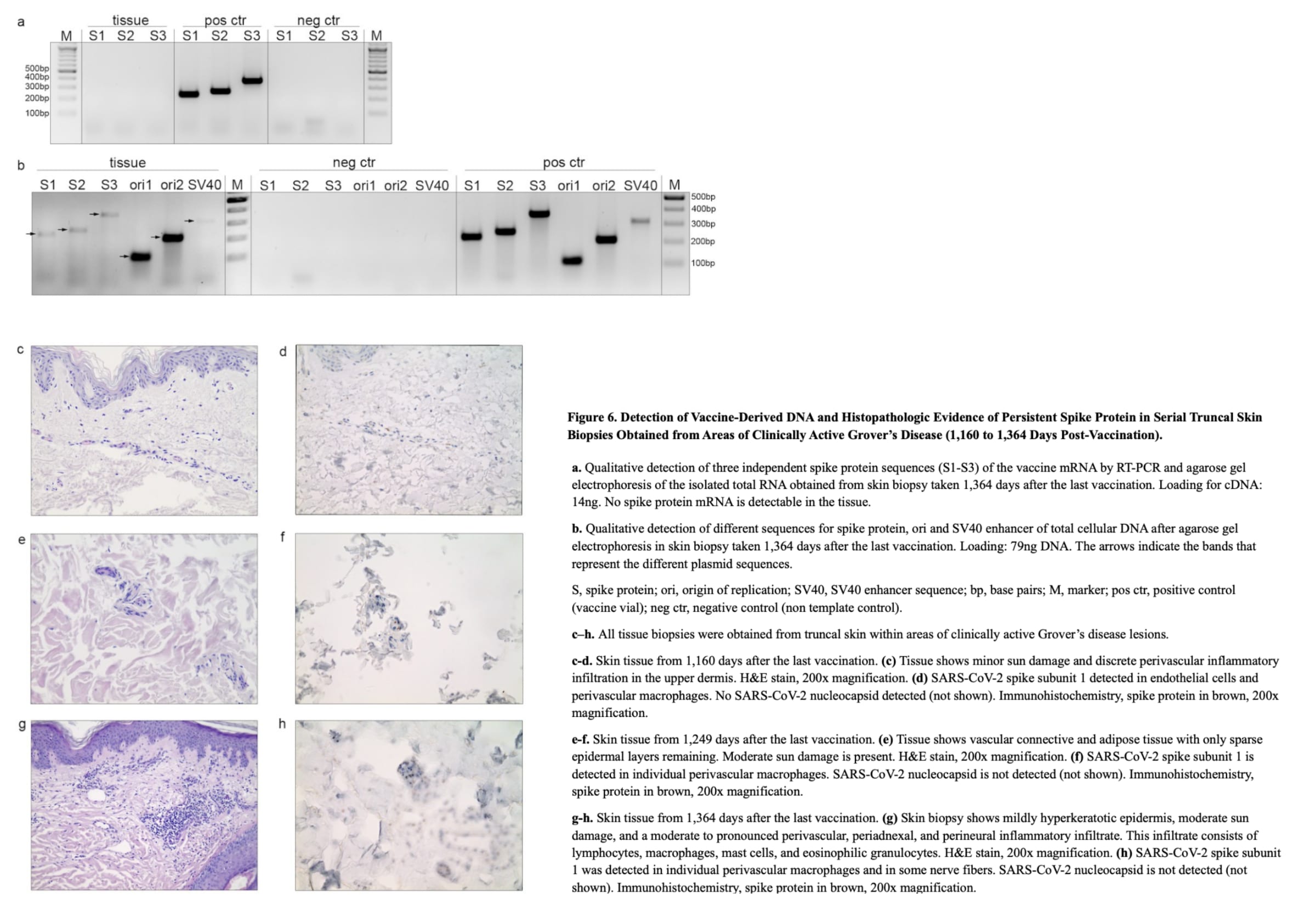
Des biopsies cutanées en série effectuées 1 160, 1 249 et 1 364 jours après la vaccination, toutes à partir de peau tronculaire dans des zones de maladie de Grover cliniquement active, se sont révélées négatives pour la nucléocapside et ont montré un dépôt persistant de protéine spike dans les cellules endothéliales et les macrophages par immunohistochimie automatisée avec corrélation histopathologique. La protéine spike a également été trouvée dans les fibres nerveuses à 1 364 jours.
La biopsie cutanée de 1 364 jours contenait de multiples éléments d’ADN plasmidique, notamment des séquences du gène spike (S1-S3), ori1/ori2 et l’amplificateur SV40, confirmant la rétention durable de l’ADN vaccinal dans le tissu somatique par amplification PCR avec électrophorèse sur gel d’agarose et séquençage Sanger.
Analyse multi-organique
L’analyse des variantes structurelles par séquençage du génome entier à 1277 jours après la vaccination a révélé une instabilité génomique généralisée, avec de grandes duplications et délétions affectant EGFR, MYC, ERBB2 et ETV6/RUNX1, tandis que la comparaison ARN-ADN a révélé des variantes ARN uniquement dans les voies ribosomales, NMD, petits ARN, épigénétiques et TP53.
Le profilage transcriptomique du sang total a mis en évidence le stress oxydatif, l’activation vasculaire et la fragilité nucléaire.
La protéomique urinaire utilisant la spectrométrie de masse quantitative a confirmé l’inflammation systémique avec suractivation du complément (CFH), déséquilibre redox (PRDX1) et réponses anticorps soutenues, appuyées par les allèles à risque HLA-B07:02 et DRB1*11:04.
Conclusion
Ce cas documente la plus longue persistance in vivo de l’ARNm, des fragments d’ADN plasmidique et de la protéine spike dérivée d’un vaccin après une vaccination à l’ARNm, avec une détection reproductible dans plusieurs laboratoires indépendants, des compartiments biologiques distincts et des systèmes de détection moléculaire complémentaires s’étendant au-delà de 3,5 ans après la dernière dose. La protéine spike, les séquences d’ARNm spike et les éléments du squelette plasmidique ont été identifiés à la fois dans les cellules immunitaires et dans les tissus somatiques, avec une absence continue de la protéine de la nucléocapside du SARS-CoV-2 ou d’anticorps, ce qui exclut effectivement l’infection antérieure comme source. La convergence de ces observations à travers un échantillonnage longitudinal de sang et de tissus fournit la preuve directe que le matériel génétique dérivé de l’ARNm d’un vaccin et ses produits protéiques traduits peuvent persister in vivo pendant des années après l’administration.
Parallèlement, des analyses multi-comiques ont révélé une instabilité génomique soutenue et une dysrégulation transcriptomique plus de 3,5 ans après la vaccination, ce qui suggère que le matériel vaccinal persistant peut être associé à des altérations à long terme des voies génomiques et moléculaires de l’hôte.
Ces données remettent en question les hypothèses dominantes concernant la dégradation rapide et l’activité biologique de courte durée des composants vaccinaux à ARNm et soulignent la nécessité de mener des études longitudinales contrôlées pour déterminer la prévalence, les mécanismes et les conséquences cliniques de la persistance du matériel dérivé des vaccins.