Relatamos a mais longa persistência documentada de componentes de vacinas de mRNA até à data, confirmada de forma independente em vários laboratórios, bioespécimes e pontos de tempo, utilizando diversos métodos analíticos.
NICOLAS HULSCHER, MPH 2 DE FEVEREIRO DE 2026
Durante anos, foi dito ao público que os materiais das vacinas de ARNm se degradariam em dias ou semanas – rapidamente decompostos, biologicamente transitórios e incapazes de persistir a longo prazo. Este pressuposto moldou as garantias regulamentares, as mensagens públicas e as expectativas de segurança em todo o mundo. Milhares de milhões de pessoas em todo o mundo receberam estas injecções com base na alegação de que o material genético desapareceria rapidamente do corpo.
Hoje, essa narrativa cai por terra – na sequência de um esforço de investigação coordenado e multinacional que envolveu a Fundação McCullough, o laboratório INMODIA (Alemanha), o Hospital Municipal de Dresden-Friedrichstadt (Alemanha), a Neo7Bioscience e laboratórios independentes colaboradores.
O artigo resultante, intitulado “Unprecedented Persistence of Vaccine mRNA, Plasmid DNA, Spike Protein, and Genomic Dysregulation Over 3.5 Years Post-COVID-19 mRNA Vaccination“, apresenta o que é, tanto quanto sabemos, o mais abrangente relatório de caso de lesão da vacina COVID-19 até à data – envolvendo >40 visitas ao departamento de emergência, >200 encontros com especialistas em 18 disciplinas médicas, >100 investigações laboratoriais, >100 estudos de imagem e amostras de sangue e tecidos em série realizadas em vários pontos de tempo ao longo de mais de 3,5 anos.
Os resultados revelam provas moleculares longitudinais de que o ARNm derivado da vacina, os fragmentos de ADN plasmídico e a proteína spike podem persistir no sangue e nos tecidos humanos mais de 3,5 anos após a vacinação – confirmados de forma independente em vários laboratórios, utilizando diversos métodos analíticos.
A infeção por SARS-CoV-2 foi efetivamente excluída: os anticorpos contra o nucleocapsídeo permaneceram negativos em cinco momentos distintos e em três laboratórios independentes, e a proteína do nucleocapsídeo estava ausente nas amostras de tecido, apesar da presença de deposição de proteína em forma de pico.
Apresentação do caso
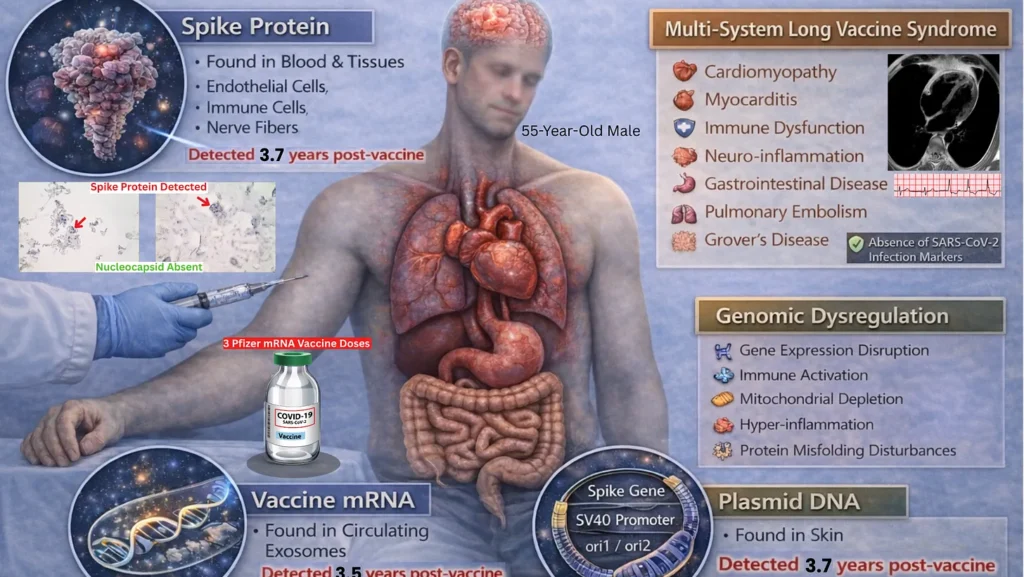
Relatamos o caso de um homem de 55 anos que recebeu três doses da vacina de ARNm contra a COVID-19 da Pfizer-BioNTech e que, subsequentemente, desenvolveu uma disfunção multiorgânica progressiva consistente com a síndrome pós-vacina contra a COVID-19 (PCVS), envolvendo os domínios cardiopulmonar, neurológico, músculo-esquelético, gastrointestinal, autonómico, otorrinolaringológico, audiovestibular, imunitário, oftalmológico, dermatológico e psiquiátrico. As manifestações clínicas incluíam: embolia pulmonar; miocardite tardia confirmada por RMN; perturbações neurocognitivas; neuropatia de pequenas fibras; disfunção autonómica; mialgia; envolvimento pancreático e gastrointestinal crónico; agravamento do zumbido com perda auditiva neurossensorial; disfagia e disfonia vocais; perturbações oftalmológicas; inflamação dermatológica crónica; e ansiedade/depressão. O caso foi avaliado através de uma investigação clínica longitudinal extensa e única, abrangendo análises moleculares, imunológicas, genéticas, proteómicas, transcriptómicas e tecidulares, realizadas para caraterizar os mecanismos da doença e excluir etiologias alternativas.
Avaliação diagnóstica exaustiva
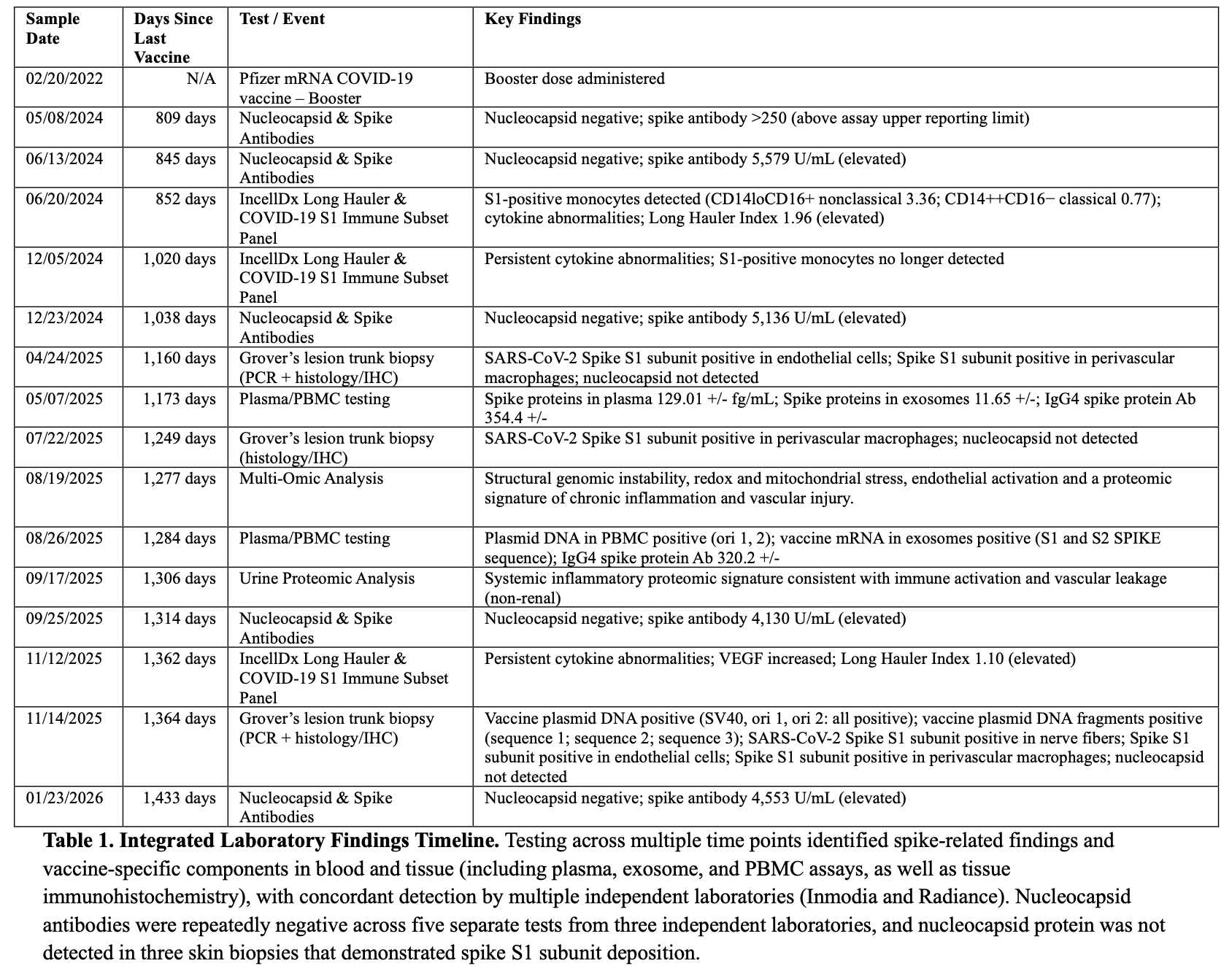
Após mais de 40 consultas no serviço de urgência e mais de 200 consultas externas de especialidade, o doente foi submetido a mais de 100 exames laboratoriais não rotineiros e a mais de 100 exames imagiológicos/funcionais. Esta avaliação excluiu sistematicamente os mecanismos etiológicos subjacentes nos domínios infecioso, autoimune, reumatológico, endócrino, genético, hematológico, maligno, tóxico/relacionado com medicamentos, cardiovascular/vascular, metabólico e neurológico primário. Os exames não foram, em grande parte, de diagnóstico. Após o diagnóstico de miocardite, suspeitou-se de uma possível infeção assintomática não documentada/diagnosticada que se manifestasse como COVID-19 longo, tendo-se prosseguido com a serologia; resultados inesperados levaram à expansão dos testes imunológicos e tecidulares para componentes derivados de picos e vacinas. Os anticorpos contra o nucleocapsídeo do SARS-CoV-2 foram negativos em cinco pontos temporais separados, abrangendo 809-1.433 dias após a vacinação, confirmados por três laboratórios independentes. O doente permanece negativo em relação ao nucleocapsídeo, com níveis persistentemente elevados de anticorpos contra o pico (4.553 U/mL) 1.433 dias após a última vacinação.
Colheita de amostras e métodos analíticos
As amostras de sangue e de tecido cutâneo foram obtidas em vários pontos temporais entre 852-1.364 dias após a vacinação final com o mRNA da COVID-19 da Pfizer-BioNTech. Os compartimentos biológicos analisados incluíram plasma, exossomas circulantes, células mononucleares do sangue periférico (PBMCs) e tecido cutâneo. Os espécimes foram avaliados em vários laboratórios independentes utilizando diversas metodologias analíticas, incluindo ELISA, imunohistoquímica automatizada, RT-PCR, PCR padrão com confirmação de sequenciação Sanger, sequenciação do genoma completo, perfil transcriptómico e espetrometria de massa quantitativa.
Proteína de pico persistente em circulação e ARNm derivado da vacina
Aos 852 dias após a vacinação, os testes imunitários baseados no sangue identificaram a deteção da proteína S1 do SARS-CoV-2 em subgrupos de monócitos clássicos e não clássicos, com anomalias associadas a citocinas e marcadores imunitários.
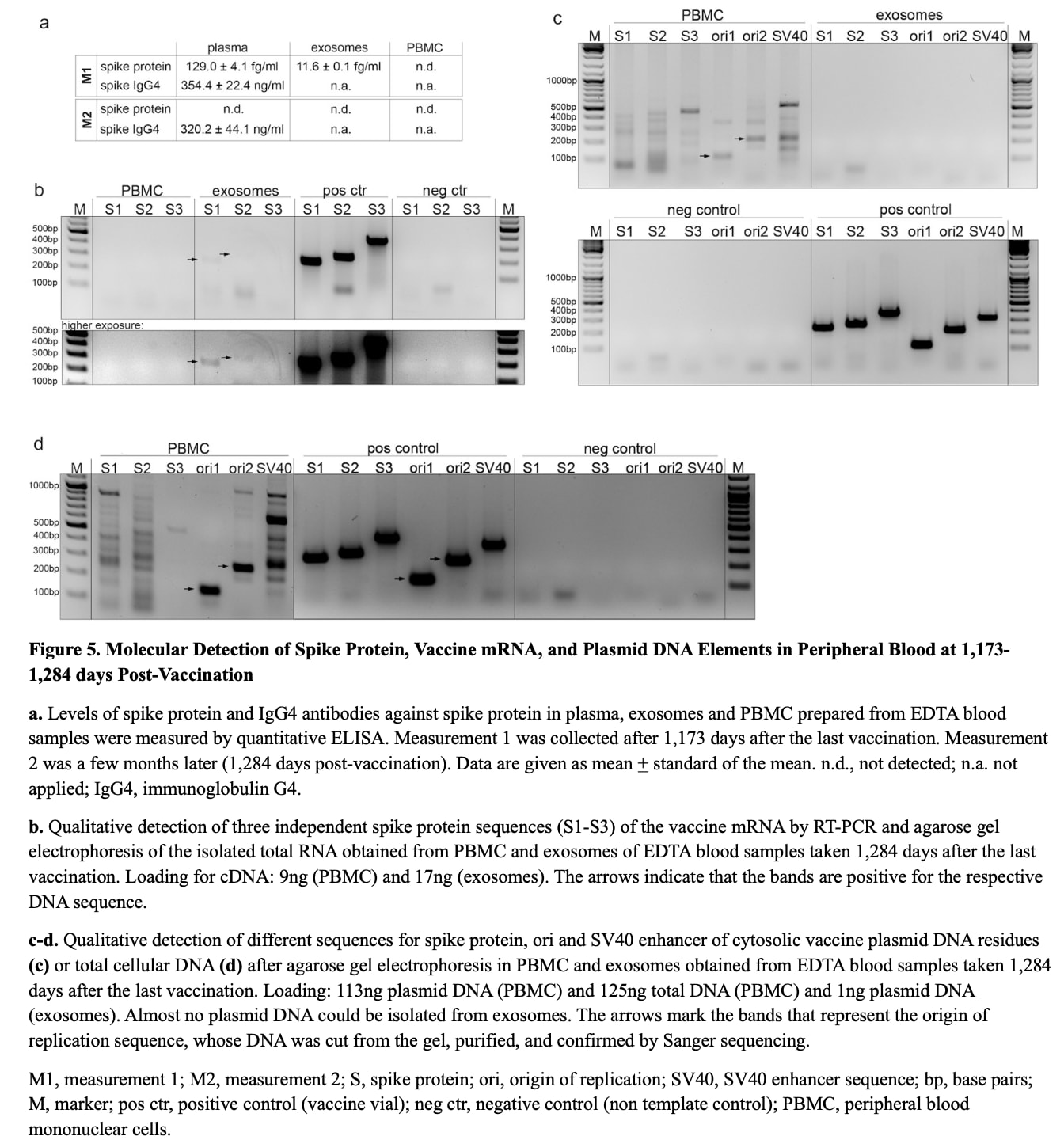
Aos 1.173 dias após a vacinação, o ELISA de alta sensibilidade detectou a proteína Wuhan spike livre no plasma (129,0 ± 4,1 fg/mL) e nos exossomas circulantes (11,6 ± 0,1 fg/mL).
Aos 1.284 dias, a RT-PCR identificou o mRNA do pico derivado da vacina nos exossomas circulantes, enquanto o RNA do PBMC permaneceu negativo após a extração tratada com DNase e a PCR específica do amplicon visando três regiões ORF do pico (S1-S3).
O perfil serológico aos 1.173 e 1.284 dias após a vacinação demonstrou concentrações persistentemente elevadas de IgG4 específicas do pico (354,4 ± 22,4 ng/mL e 320,2 ± 4,4 ng/mL, respetivamente), consistentes com a estimulação antigénica contínua e uma resposta enviesada de imunotolerância.
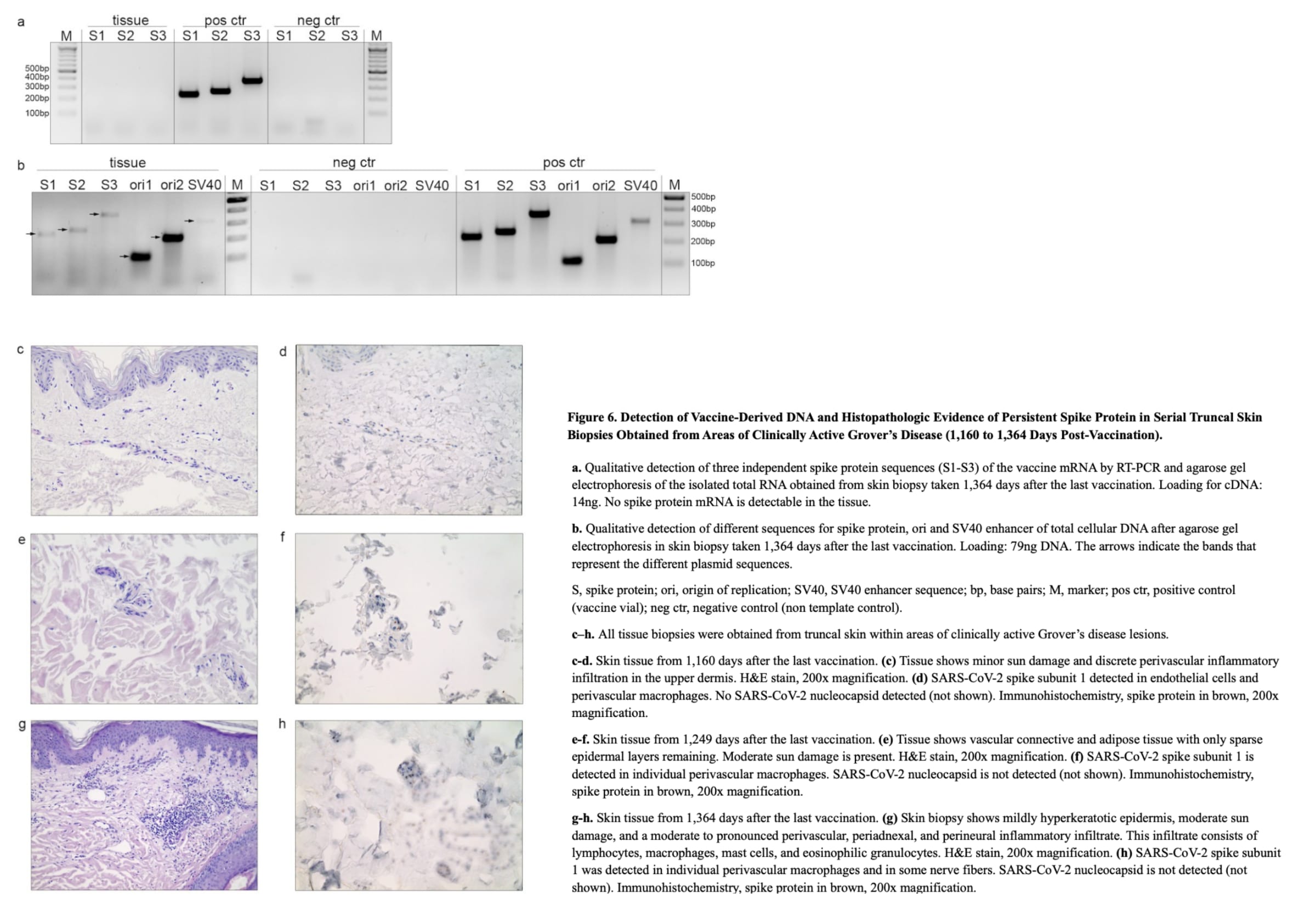
Proteína Spike Persistente e ADN Plasmídico em Tecido Cutâneo
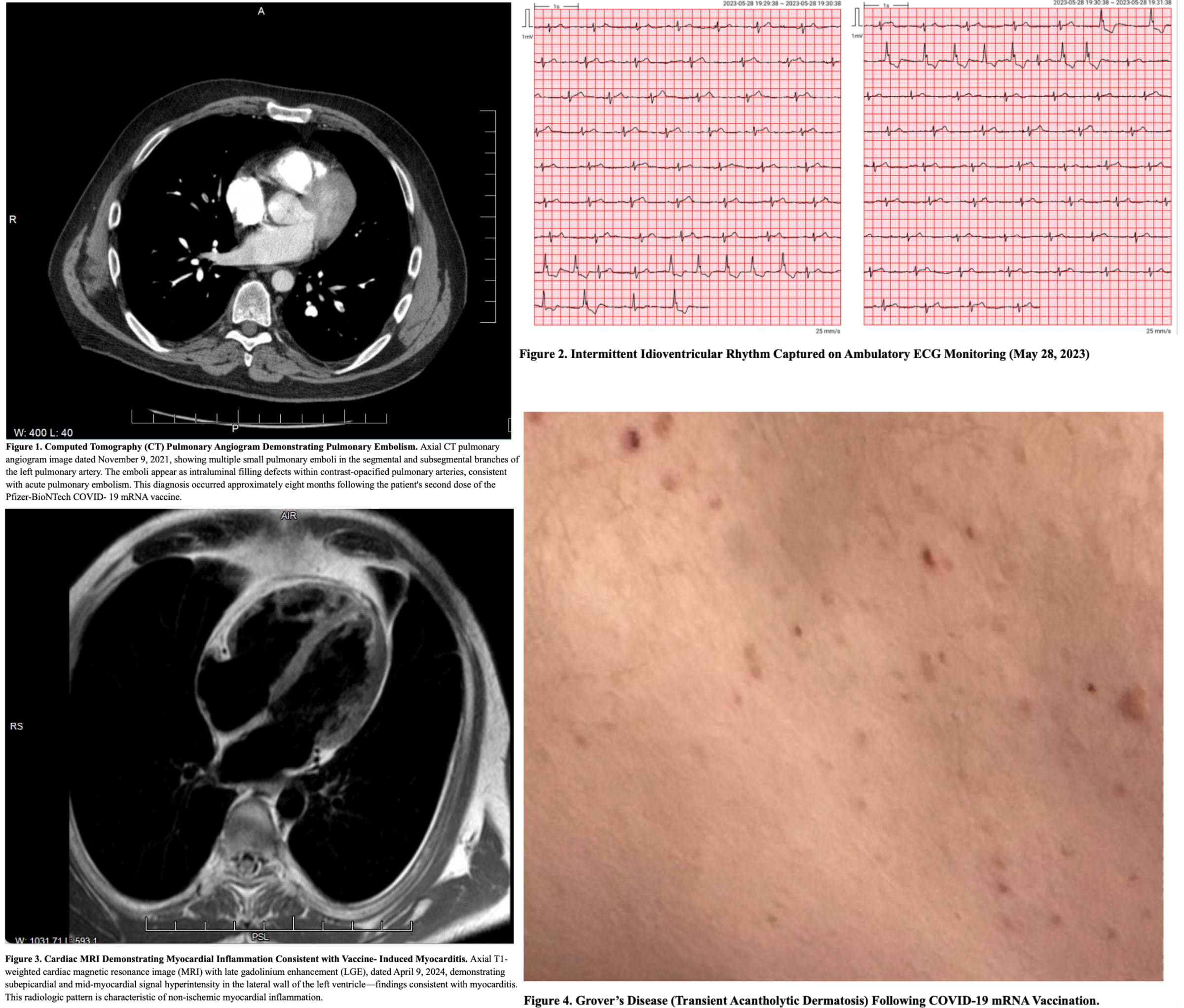
Biópsias cutâneas seriadas aos 1160, 1249 e 1364 dias após a vacinação, todas de pele truncal em áreas de doença de Grover clinicamente ativa, foram negativas para o nucleocapsídeo e demonstraram deposição persistente de proteína spike em células endoteliais e macrófagos por imunohistoquímica automatizada com correlação histopatológica. A proteína Spike também foi encontrada nas fibras nervosas aos 1.364 dias.
A biópsia cutânea de 1364 dias continha múltiplos elementos de ADN plasmídico, incluindo sequências do gene spike (S1-S3), ori1/ori2 e o potenciador SV40, confirmando a retenção duradoura do ADN derivado da vacina no tecido somático através da amplificação por PCR com eletroforese em gel de agarose e sequenciação Sanger.
Análise Multi-Ómica
A análise de variantes estruturais por sequenciação de todo o genoma, 1.277 dias após a vacinação, revelou uma instabilidade genómica generalizada, com grandes duplicações e supressões que afectam EGFR, MYC, ERBB2 e ETV6/RUNX1, enquanto a comparação RNA-DNA mostrou variantes apenas de RNA nas vias ribossómica, NMD, RNA pequeno, epigenética e TP53.
O perfil transcriptómico do sangue total evidenciou o stress oxidativo, a ativação vascular e a fragilidade nuclear.
A proteómica da urina utilizando espetrometria de massa quantitativa confirmou inflamação sistémica com sobreactivação do complemento (CFH), desequilíbrio redox (PRDX1) e respostas sustentadas de anticorpos, apoiadas por alelos de risco HLA-B07:02 e DRB1*11:04.
Conclusão
Este caso documenta a mais longa persistência in vivo relatada de mRNA derivado da vacina, fragmentos de DNA plasmídeo e proteína spike após a vacinação de mRNA, com deteção reprodutível em vários laboratórios independentes, compartimentos biológicos distintos e sistemas de deteção molecular complementares que se estendem além de 3,5 anos após a dose final. A proteína spike, as sequências de mRNA spike e os elementos da espinha dorsal do plasmídeo foram identificados tanto em células imunitárias como em tecido somático, com ausência continuada da proteína do nucleocapsídeo do SARS-CoV-2 ou de anticorpos, excluindo efetivamente a infeção anterior como fonte. A convergência destas observações através da amostragem longitudinal de sangue e tecido fornece evidência direta de que o material genético derivado da vacina de ARNm e os seus produtos proteicos traduzidos podem persistir in vivo durante anos após a administração.
Paralelamente, as análises multi-ómicas revelaram uma instabilidade genómica sustentada e uma desregulação transcriptómica mais de 3,5 anos após a vacinação, sugerindo que o material persistente derivado da vacina pode estar associado a alterações a longo prazo nas vias genómicas e moleculares do hospedeiro.
Estes dados desafiam os pressupostos prevalecentes sobre a rápida degradação e a atividade biológica de curta duração dos componentes da vacina de ARNm e sublinham a necessidade de estudos longitudinais controlados para determinar a prevalência, os mecanismos e as consequências clínicas do material persistente derivado da vacina.